
उपसहसंयोजक यौगिकों में समावयवता
समावयवता – ऐसे यौगिक जिनके अणुसुत्र समान हो लेकिन भौतिक एवं रासायनिक गुणों में भिन्नता हो उन्हें समावयवी यौगिक तथा इस गुण को समावयवता कहते है।
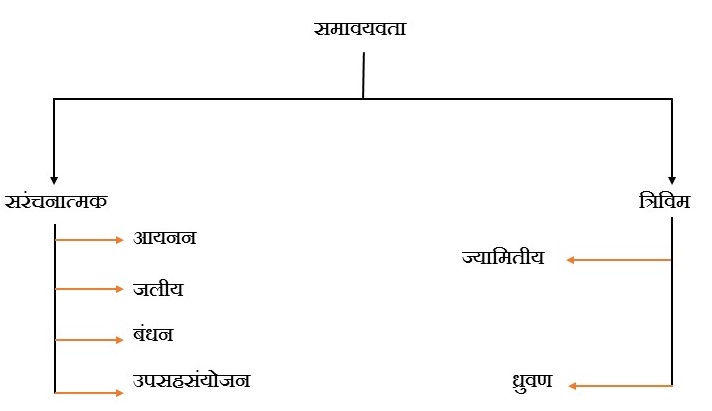
सरंचनात्मक समावयवता
आयनन समावयवता – इस प्रकार की समावयवता में आयनों का उपसहसंयोजन क्षेत्र से आयनन क्षेत्र में तथा आयनन क्षेत्र से उपसहसंयोजन क्षेत्र में आदान प्रदान होता है इस प्रकार की समावयवता का पता मूलक परीक्षण से करते है।
[Co(NH3)5Br] → [Co(NH3)5SO4]Br
AgNO3 में मिलाने से कोई अवक्षेप नही AgNO3 में मिलाने पर अवक्षेप आता है
BaCl2 में मिलाने पर अवक्षेप आता है BaCl2 में मिलाने से कोई अवक्षेप नही
वे यौगिक जिनके अणुसुत्र समान हो तथा जो जलीय विलयन में भिन्न भिन्न प्रकार के आयन देते है आयनन समावयवी कहलाते है।
Q.निम्न संकुल किस प्रकार की समावयवता प्रदर्शित करते है व इसका पता कैसे लगाओगे ?
- [Co(NH3)2 (H2O)2Br2]Cl → [Co(NH3)2 (H2O)2BrCl]Br
AgNO3 मिलाने पर AgCl का सफ़ेद अवक्षेप आता है AgNO3 मिलाने पर AgBr का हल्का पीला अवक्षेप आता है
अर्थात आयनन समावयवता
- [Co(NH3)5(NO3) ]SO4 → [Co(NH3)5(SO4)] NO3
- [CoCl (NO2) (NH3)4]Cl → [CoCl2(NH3)4]NO2
जलीय समावयवता – यदि किसी समावयवी में जल का अणु आयनन से उपसहसंयोजन क्षेत्र में आता है तो इस प्रकार की समावयवता को जलीय समावयवता कहते है।
[Co(NH3)3Cl3] .3H2O
↓
[Co(NH3)3(H2O)Cl2]Cl .2H2O
↓
[Co(NH3)3(H2O)2Cl]Cl2 .H2O
बंधन समावयवता – इस प्रकार की समावयवता उभय दंतुक लिगेंड व्यक्त करते है तथा इस प्रकार के समावयवियो में केवल दाता परमाणु की स्थिति परिवर्तित होती है।
- [Co(NO2)2(NH3)4]Cl → [Co(ONO)2(NH3)4]Cl
- NH4[Co(NH3)2(NCS)4] → NH4[Co(NH3)2(SCN)4]
- [Fe(CN)6]4- → [Fe(NC)6]4-
उपसहसंयोजन समावयवता – इस प्रकार की समावयवता वे यौगिक दर्शाते है जिनमे एक धनायनिक व ऋणायनिक संकुल उपस्थित हो।
1.जब दोनों धातु आयन भिन्न भिन्न हो
इस प्रकार की समावयवता में दोनों धातु परमाणुओं के लिगेंडो को आपस में प्रतिस्थापित करते है।
[Cr(NH3)6][Co(CN)6] → [Co(NH3)6][Cr(CN)6]
[Pt(NH3)4][CuCl4] → [Cu(NH3)4][PtCl4]
2.जब दोनों धातु आयन समान हो
यदि दोनों धातु आयन समान हो तो उस समय केवल उतने ही लिगेंड परिवर्तित करते है जब तक की दोनों संकुल भिन्न भिन्न अवस्था में रहे।
उदाहरण -1 [Pt(py)][PtCl4]
↓
[Pt(py)3][PtCl3(py)]
उदाहरण -2.
[Cr(NH3)6][Cr(CN)6]
↓
[Cr(NH3)5(CN)][Cr(CN)5(NH3)]
↓
[Cr(NH3)4(CN)2][Cr(CN)4(NH3)2]
https://hi.wikipedia.org/wiki/
उम्मीद है आपको उपसहसंयोजक यौगिकों में समावयवता TOPIC अच्छा लगा होगा इसी तरह आप जुड़े रहिये हमारे साथ WWW.EDUCATIONALERT.IN
Good
सर जी आपके नोट्स बहुत ही आसान ओर अच्छे हैं
शुक्रिया सर जी हमारे लिए इतनी मेहनत करने के लिए ।
Thanks….
Good notes
VERY GOOD NOTES