
विलयन का वाष्पदाब
अवाष्पशील ठोस का द्रव में विलयन का वाष्पदाब
शुद्ध विलायक में विलायक की सतह से वाष्पशील होने वाले कणों की संख्या अधिकतम होती है और विलायक का वाष्प दाब भी अधिक होता है। अवाष्पशील विलेय मिलाने के बाद सतह पर उपस्थित विलायक के कणों के बीच-बीच में विलय के कण भी आ जाते हैं,अतः सतह को छोड़कर वाष्प में बदलने वाले कणों की संख्या कम हो जाती है जिससे विलयन में विलायक का वाष्प दाब कम हो जाता है इस प्रकार के विलयनों में क्योंकि विलेयअवाष्पशील है विलयन का कुल वाष्प दाब सिर्फ विलायक के कारण ही होता है।

हेनरी का नियम राउल्ट के नियम की विशेष स्थिति
हेनरी के नियमानुसार “द्रव्य की सतह पर द्रव गैस का आंशिक दाब द्रव में घुले हुए गैस के मोल भिन्न के समानुपाती होता है”।
राउल्ट के नियमानुसार “दो वाष्पशील द्रवों के विलयन में एक घटक का वाष्प दाब विलयन में उसके मॉल भिन्न के समानुपाती होता है”।

हेनरी के नियम में गैस ही अत्यधिक वाष्पशील होने के कारण मुख्यतः दाब डालती है अतः जब का KH मान p0 के बराबर होता है तो हेनरी का नियम राउल्ट का नियम बन जाता है।
आदर्श विलयन – आदर्श विलयन ऐसे विलयन जो सभी सांद्रताओं पर राउल्ट के नियम का पालन करते है तथा जिनके लिए ΔH एवं ΔV का मान शून्य होता है आदर्श विलयन कहलाते है। ΔH = उर्जा में परिवर्तन की दर , ΔV = आयतन में परिवर्तन की दर
माना घटक A एवं B को मिलाकर विलयन बनाया जाता है शुद्ध घटक A के कणों के बीच में अन्योन्य क्रियाएं A–A प्रकार की होगी शुद्ध घटक के कणों के बीच में B–B प्रकार की अन्योन्य क्रियाएं होगी और विलयन बनाने के बाद विलयन में A–B प्रकार की अन्योन्य क्रियाएं भी उपस्थित होगी यदि A–B प्रकार की अन्योन्य क्रियाएं A–A प्रकार की अन्योन्य क्रियाओं तथा B–B प्रकार की अन्योन्य क्रियाओं के समान ही है तो आदर्श विलयन बनते है।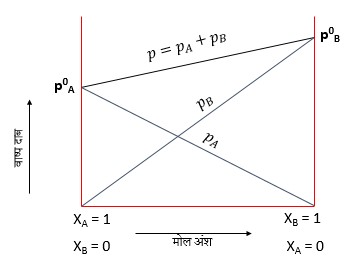
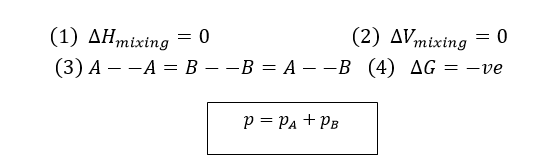 उदाहरण –
उदाहरण –
(1-Propanole , 2-Propanole) (n-Hexane , n-Heptane) (Bromo Ethane , Chloro Ethane) (Benzene , Toluene)
Great Work
Great sir ji🙌🙏