
द्रव विलयनों का वाष्प दाब
सामान्य ताप पर प्रत्येक द्रव कुछ न कुछ वाष्पशील होता है यदि द्रव को बंद पात्र में लिया जाए तो इसकी वाष्प द्वारा द्रव की सतह पर डाला गया दाब ही वाष्प दाब कहलाता है।
[साम्य अवस्था में जब वाष्पीकरण की दर संघनन की दर की बराबर हो जाए]
द्रव–द्रव विलयनों का वाष्प दाब
विलयनों के वाष्प दाब को समझाने के लिए वैज्ञानिक राउल्ट ने नियम दिया ।
राउल्ट का नियम
“माना दो वाष्पशील द्रवों का एक द्विअंगी विलयन बनाया जाता है राउल्ट के नियम अनुसार दो वाष्पशील द्रव के विलयन में प्रत्येक घटक का वाष्प दाब विलयन में उसके मोल अंश के समानुपाती होता है”
यदि प्रत्येक घटक को A व B के द्वारा प्रदर्शित करें तो राउल्ट के नियमानुसार

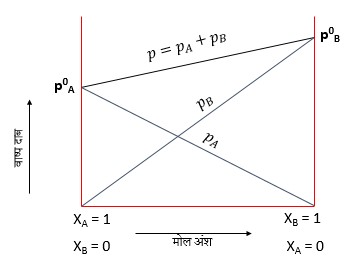
उपरोक्त समीकरण तथा ग्राफ से निम्न निष्कर्ष निकलते है।
- दो वाष्पशील द्रवों के विलयन के कुल वाष्पदाब को विलयन में उपस्थित एक घटक की मोल भिन्न से सम्बंधित कर सकते है।
- विलयन का कुल वाष्पदाब प्रत्येक घटक की मोल भिन्न के साथ रेखीय रूप से परिवर्तित होता है।
- विलयन के कुल वाष्पदाब का न्यूनतम मान P0A व अधिकतम मान P0B है यहाँ यह माना गया है कि घटक B , A से ज्यादा वाष्पशील है।
- किसी भी द्रव का शुद्ध अवस्था में वाष्पदाब अधिकतम होता तथा इसका दूसरे द्रव के साथ विलयन बनाने पर इसके वाष्पदाब में हमेशा कमी आती है।
दो वाष्पशील द्रवों के विलयन में विलयन पर उपस्थित इनकी वाष्प प्रावस्था का संघठन निम्न सूत्रों की सहायता से ज्ञात किया जा सकता है।
PA =YA .Ptotal
PB =YB .Ptotal
जहाँ
PA = घटक A का विलयन में आंशिक दाब , PB = घटक B का विलयन में आंशिक दाब
YA = घटक A का वाष्प अवस्था में मोल भिन्न ,YB = घटक B का वाष्प अवस्था में मोल भिन्न
Nice
Great Work 👍 👍👍👍👍