कोलाइडो का वर्गीकरण
कोलाइडो का वर्गीकरण –
- परिक्षिप्त प्रावस्था व परिक्षेपण माध्यम की भौतिक अवस्था के आधार पर
इस आधार पर कोलाइडी विलयन आठ प्रकार के होते हैं।
| क्र. सं. | परिक्षिप्त प्रावस्था | परिक्षेपण माध्यम | कोलाइड | उदाहरण |
| 1 | ठोस | ठोस | ठोस सॉल | रंगीन कांच |
| 2 | ठोस | द्रव | सॉल | पेंट , स्याही |
| 3 | ठोस | गैस | एरोसॉल | धुँआ, धूल |
| 4 | द्रव | ठोस | जैल | पनीर ,मक्खन |
| 5 | द्रव | द्रव | इमल्शन (पायस) | दूध |
| 6 | द्रव | गैस | एरोसॉल | धुंध ,कोहरा, बादल |
| 7 | गैस | ठोस | ठोस सॉल | फोम ,समुद्री झाग |
| 8 | गैस | द्रव | फोम | साबुन के झाग |
2. परिक्षिप्त प्रावस्था व परिक्षेपण माध्यम के बीच अन्योन्य क्रिया के आधार पर
- द्रवस्नेही (द्रवरागी) कोलाइड
जब परिक्षिप्त प्रावस्था के कण द्रव परिक्षेपण माध्यम में घुलने की प्रवृत्ति रखते हैं तो इन दोनों को मिलाकर तैयार किया गया सॉल द्रवस्नेही (द्रवरागी) कोलाइड कहलाता है यदि परिक्षेपण माध्यम को परिक्षिप्त प्रावस्था से अलग कर दिया जाए तो सॉल को केवल परिक्षेपण माध्यम के साथ मिलाकर पुनः प्राप्त किया जा सकता है अतः इनको उत्क्रमणीय सॉल भी कहते हैं। द्रवस्नेही = द्रव से स्नेह करने वाला
उदाहरण – गोंद को जल में मिलाने पर द्रवस्नेही (द्रवरागी) का निर्माण होता है।
- द्रवविरोधी (द्रवविरागी) कोलाइड
जब ठोस परीक्षित प्रावस्था के कण द्रव परिक्षेपण माध्यम में मिलाए जाते हैं तो सॉल तैयार नहीं होता है इनके लिए विशेष विधियां अपनाई जाती हैं क्योंकि परिक्षिप्त प्रावस्था के कण परिक्षेपण माध्यम में घुलने की प्रवृत्ति नहीं रखते हैं ऐसे सॉल को द्रवविरोधी (द्रवविरागी) सॉल कहते हैं । यह प्रक्रम अनुत्क्रमणीय होता है अर्थात एक बार अवक्षेपित होने के बाद यह केवल परिक्षेपण माध्यम के मिलाने से ही कोलाइडी सॉल नहीं देते हैं।
उदाहरण – सल्फर सॉल, गोल्ड सॉल
नोट – पानी को परिक्षेपण माध्यम में लेकर बनाए गए सोल्को एक्वसॉल या हाइड्रोसॉल कहा जाता है।
द्रवस्नेही (द्रवरागी) कोलाइड द्रवविरोधी (द्रवविरागी) कोलाइड में अंतर
| द्रवस्नेही (द्रवरागी) कोलाइड | द्रवविरोधी (द्रवविरागी) कोलाइड |
| ये आसानी से बनाये जा सकते है। | ये विशेष विधियों द्वारा बनाये जाते है। |
| ये उत्क्रमणीय होते है। | ये अनुत्क्रमणीय होते है। |
| ये अल्ट्रा माइक्रोस्कोप द्वारा आसानी से नहीं देखे जा सकते है। | ये अल्ट्रा माइक्रोस्कोप द्वारा आसानी से देखे जा सकते है। |
| ये स्वतः स्थाई होते है। | ये अस्थाई होते है अर्थात स्थाईत्व हेतु स्थाईत्व प्रदान करने वाले कारक मिलाते है। |
| ये विधुत अपघट्य की अधिक मात्रा मिलाने पर ये अवक्षेपित हो जाते है जिसे स्कंदन कहते है। | ये विधुत अपघट्य की सूक्ष्म मात्रा मिलाने पर ये अवक्षेपित हो जाते है। |
| ये टिंडल प्रभाव नहीं दर्शाते है। | ये टिंडल प्रभाव दर्शाते है। |
| ये विलायक के प्रति आकर्षण के कारण अत्यधिक जलयोजित होते है। | द्रव विरोधी होने के कारण इनमें जलयोजन नहीं होता है। |
- परिक्षिप्त प्रावस्था के कणों के आधार पर
1.बहुआणविक कोलाइड
जब किसी कोलाइड में प्रत्येक कोलाइडी कण परिक्षिप्त प्रावस्था के कई कणों (परमाणु व अणुओं) से मिलकर बना होता है अर्थात कई कण आपस में जुड़कर कोलाइडी आकार के कण बनाते हैं।
उदाहरण – सल्फर सॉल (इसमें प्रत्येक कोलाइडी कण में 1000 से भी ज्यादा S8 कण होते हैं)
2.वृहद आणविक कोलाइड
इस प्रकार के कोलाइड में प्रत्येक कोलाइडी कण एक ही अणु होता है जो कि कुछ बड़े आकार के अणुओं के कोलाइडी से ही संबंधित है।
उदाहरण – प्रोटीन,सैलूलोज, स्टार्च ,पॉलिथीन, नायलॉन आदि के सॉल वृहद आणविक कोलाइड कहलाते हैं।
3.सहचारी कोलाइड
कुछ पदार्थों के ऐसे कोलाइड बनते हैं जो एक निश्चित ताप से अधिक ताप पर (जिसे क्राफ्ट ताप कहते हैं) तथा एक निश्चित सांद्रता से अधिक सांद्रता (क्रांतिक मिशेल सांद्रता (CMC)) पर बनते हैं या स्थाई होते हैं उन्हें सहचारी कोलाइड कहते हैं । क्राफ्ट ताप पर तथा क्रांतिक मिसेल सांद्रता से अधिक सांद्रता पर कोलाइडी विलयन में उपस्थित कोलाइडी कर मिसेल कहलाते हैं।
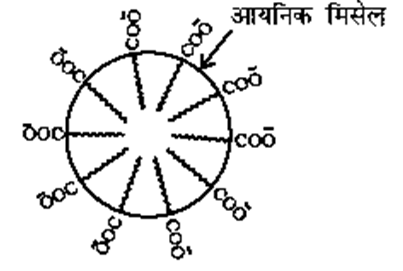
साबुन के लिए क्रांतिक मिसेल सांद्रता का मान 10-4 से 10-3 MolL-1 होता है।
उदाहरण – साबुन और अपमार्जक को जल में मिलाने पर यह सहचारी कोलाइड ही बनाते हैं इन कोलाइडो में द्रवरागी व द्रवविरागी दोनों ही भाग होते हैं।
साबुन – साबुन उच्च कार्बन परमाणु वाले संतृप्त वसीय अम्लों के सोडियम अथवा पोटैशियम लवण होते हैं इन्हें RCOO–Na+ सूत्र से व्यक्त करते हैं।
सोडियम स्टीयरेट एक सामान्य प्रकार का साबुन होता है जो कि स्टीयरिक अम्ल का सोडियम लवण होता है।

मिसेल निर्माण की क्रियाविधि
जब साबुन को जल में मिलाते हैं तो जल में आयनित हो जाता है। इस प्रकार साबुन का ध्रुवीय सीरा जल में विलयशील होता है तथा अध्रुवीय सीरा कांटो के रूप में बाहर निकला रहता है जब जल में साबुन की सांद्रता बढ़ाते हैं तो CMC से अधिक सांद्रता पर अध्रुवीय सीरे वांडरवाल्स आकर्षण बलों की वजह से अंदर खींच जाते हैं तथा छोटे-छोटे आकार के कोलाइडी आकार के कण बनते हैं जिन्हें मिसेल कहते हैं।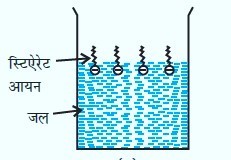
साबुन के शोधन की प्रक्रिया
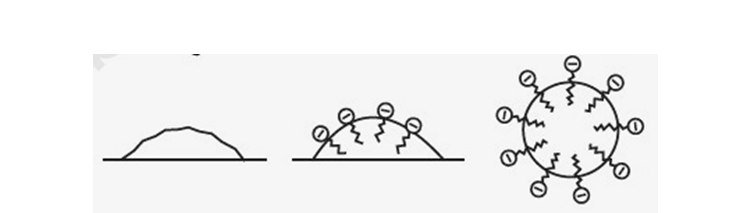
जब साबुन मिले हुए जल को चिकनाई लगे हुए कपड़ों पर लगाया जाता है तो इस तेल या चिकनाई से साबुन का अध्रुवीय सीरा (हाइड्रोकार्बन सीरा) जुड़ जाता है जबकि आयनिक सिरा जल के साथ जुड़ता है इस प्रकार यह जुड़कर मिसेल का निर्माण कर लेते हैं अर्थात साबुन के कई अणु तैलीय पदार्थ या चिकनाई को चारों तरफ से घेर लेते हैं जब कपड़ों को रगड़कर साफ करते हैं तो तैलीय मैल या चिकनाई मिसेल के द्वारा खींच कर बाहर आ जाते हैं और कपड़े साफ हो जाते हैं।
कोलाइडो का वर्गीकरण