अभिक्रियावेग पर तापका प्रभाव
अभिक्रिया वेग पर ताप का प्रभाव (अभिक्रिया वेग की ताप पर निर्भरता)
किसी रासायनिक अभिक्रिया का वेग तप्ताप बढ़ाने पर बढ़ता है तथा वेग स्थिरांक का मान भी बढ़ जाता है यह पाया गया है कि किसी रासायनिक अभिक्रिया में ताप वृद्धि से वेग स्थिरांक में लगभग दुगुनी वृद्धि हो जाती है अभिक्रिया वेग की ताप पर निर्भरता की व्याख्या आर्रेनियस समीकरण से की जा सकती है।
आर्रेनियस का सिद्धांत
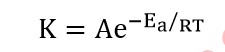
A = पूर्व चर घातांकी गुणांक ,T = परम ताप , Ea = सक्रियण उर्जा , R = गैस स्थिरांक , K = वेग स्थिरांक , E = चर घातांकी गुणांक
प्रमुख बिंदु
1.रासायनिक अभिक्रिया में अभिकारको के सभी अणु रासायनिक अभिक्रिया में भाग लेते है क्रियाकारको के कुल अणुओं की संख्या का वह अंश जो रासायनिक अभिक्रिया में भाग लेते है सक्रीय अणु कहलाते है तथा शेष निष्क्रिय अणु कहलाते है सक्रिय अणु जो अभिक्रिया के उर्जा रोधक को पार कर लेते है।
2.क्रियाकारको के अणुओं को क्रिया करने के लिए न्यूनतम उर्जा की आवश्यकता होती है क्रियाकारको के अणुओं की औसत ऊर्जा से अधिक अतिरिक्त ऊर्जा जो कि क्रिया करने के लिए आवश्यक होती है सक्रियण ऊर्जा कहलाती है।
3.क्रियाकारको के अणु परस्पर टक्करों द्वारा आवश्यक सक्रियण ऊर्जा प्राप्त कर सक्रिय हो जाते है।
4.सक्रिय अणु आपस में टकराकर उच्च ऊर्जा एवं दुर्बल बंधो का अस्थायी यौगिक बनाते है जिसे सक्रीयत संकर (संक्रमण अवस्था) कहते है सक्रीयत संकर टूटकर उत्पाद बनाता है।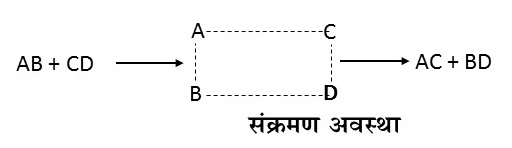
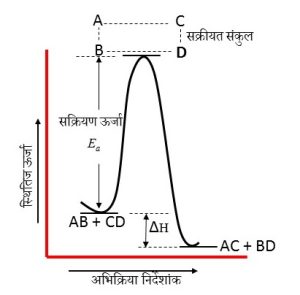
आर्रेनियस समीकरण

अभिक्रियावेग पर तापका प्रभाव








4 Comments