
क्रिस्टलीय ठोसों का वर्गीकरण
क्रिस्टलीय ठोसों का वर्गीकरण
1. आयनिक ठोस — इनमें अवयवी कण आयन होते हैं अर्थात विपरीत आवेश होने पर प्रबल स्थिर विधुत आकर्षण बल से बंधे रहते है यह ठोस कठोर,भंगुर,गलनांक और क्वथनांक उच्च व ठोस अवस्था में विधुत के कुचालक व गलित अवस्था में विद्युत का चालन करते हैं
उदाहरण(Examples) — NaCl ,CuSO4 ,KClO3
- धात्विक ठोस
इसमें धातु परमाणु प्रबल धात्विक बंध द्वारा जुड़े रहते हैं इसमें धनायन मुक्त इलेक्ट्रॉनों के समुद्र में व्यवस्थित रहते हैं इलेक्ट्रॉन गतिशील तथा क्रिस्टल में समान रूप से फैले रहते हैं इन इलेक्ट्रॉनों के कारण धातुएं विद्युत व ऊष्मा की सुचालक होती है धातुएं अघातवर्धनीय एवं तन्य होती है अर्थात इनकी चादर बनाई जा सकती है l
उदाहरण(Examples) —Cu ,Au, Ag, Al, Fe
3. आणविक ठोस
यह तीन प्रकार के होते हैं l
(A) अध्रुवीय आणविक ठोस
अवयवी अणुओं में अध्रुवीय सहसंयोजक बंध होते हैं विधुत के कुचालक, मुलायम कमरे के ताप पर द्रव एवं गैस होते हैं l
उदाहरण(Examples) —Cl2 ,N2, O2, H2, I2, CO2 (विधुत के कुचालक सभी)
(B) ध्रुवीय आणविक ठोस
अवयवी अणुओं के मध्य ध्रुवीय सहसंयोजक बंध उपस्थित होते हैं यह मुलायम कमरे के ताप पर द्रव/ गैस विधुत के सभी कुचालक होते हैं l
उदाहरण(Examples) —HCl, NH3, SO2 (विधुत के कुचालक सभी)
(C) हाइड्रोजन बंध आणविक ठोस
अवयवी अणुओं के मध्य हाइड्रोजन बंध होता है यह मुलायम ,कमरे के ताप पर वाष्पशील द्रव या ठोस होते हैं l
उदाहरण(Examples) —HF, H2O, R-OH (विधुत के कुचालक सभी)
- सह संयोजक या नेटवर्क ठोस
इस प्रकार के ठोस ओं में अवयवी कणों के मध्य प्रबल सहसंयोजक बंधो का त्रिविम जाल पाया जाता है l जिसके कारण यह अत्यधिक कठोर होते हैं गलनांक उच्च व विद्युत के सामान्यतः कुचालक होते हैं l
अपवाद — ग्रेफाइट (सुचालक)
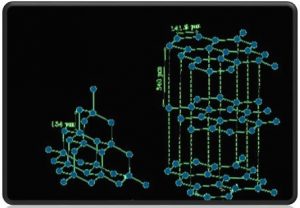
उदाहरण(Examples) — हीरा, ग्रेफाइट, फुलरीन, AlN, SiC
NOTE- प्रकृति में पाया जाने वाला कठोरतम पदार्थ हीरा है l
NOTE–
- अक्रिस्टलीय ठोस गर्म करने पर क्रिस्टलीय ठोस में परिवर्तित सकते है प्राचीन सभ्यता की कांच की सामग्री में दूधियापन पाया जाता है क्योंकि कांच के कुछ भाग का क्रिस्टलीकरण हो जाता है l
- अक्रिस्टलीय ठोसों में द्रवों के समान धीमे–धीमे बहने का गुण होता है इसलिए इसे आभासी ठोस या अतिशीतित द्रव भी कहा जाता है l
Thanku so much