क्रिस्टल क्षेत्र सिद्धांत
प्रतिपादनकर्ता – हंस बेथे के द्वारा विकसित
एवं 1930 के दशक में जोन हैस्ब्रुक वैन वेलेक
VBT की कमियों को दूर करने के लिए इन वैज्ञानिकों ने CFT सिद्धांत का प्रतिपादन किया।
- यह सिद्धांत लिगेंड को अधिक महत्त्व देता है न की केन्द्रीय धातु परमाणु को ।
- इस सिद्धांत के अनुसार धातु तथा लिगेंड के मध्य बना बंध पूर्णतया सहसंयोजक न होकर आयनिक प्रकृति का होता है।
- इन संकुलों के बनते समय d- कक्षक विपाटित हो जाते है तथा इस विपाटन में प्रयुक्त ऊर्जा को क्रिस्टल क्षेत्र विपाटन ऊर्जा (CFSE) कहते है।
- d- कक्षको का विभाजन लिगेंड की प्रकृति पर निर्भर करता है।
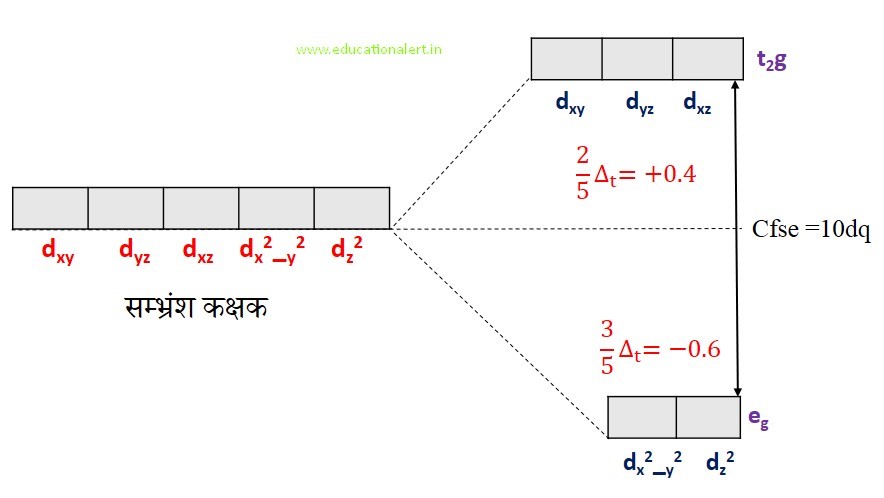
अष्टफलकीय संकुल यौगिकों में d –कक्षको का विपाटन
अष्टफलकीय संकुल यौगिकों में जब लिगेंड को d –कक्षको की और बढ़ाया जाता है तो अक्षीय d- कक्षक (dx2-y2 ,dz2) (eg) की ऊर्जा में वर्द्धि हो जाती है क्योंकि लिगेंड के इलेक्ट्रॉनों तथा इन कक्षको के मध्य प्रतिकर्षण होता है इनमे d- कक्षक की पालियां अक्षो के ऊपर विन्यासित होती है जबकि अन अक्षीय d- कक्षक (dxy ,dyz ,dzx) (t2g) में d – कक्षक की पालियां अक्षो के मध्य विन्यासित होने के कारण लिगेंड के इलेक्ट्रॉन से प्रतिकर्षित नही हो पाते है अतः t2g कक्षक निम्न ऊर्जा स्तर में तथा eg कक्षक उच्च ऊर्जा स्तर में भरे जाते है।
इस विपाटन में चौथा इलेक्ट्रॉन t2g में जायेगा या eg में जायेगा यह क्रिस्टल क्षेत्र विपाटन (Δo) और युग्मन ऊर्जा (P) के तुलनात्मक अंतर पर निर्भर करता है।
- क्रिस्टल क्षेत्र विपाटन (Δo) > युग्मन ऊर्जा (P) हो तो इलेक्ट्रॉन t2g कक्षक में जायेगा तथा जिन लिगेंड के कारण ऐसा होता है वे प्रबल क्षेत्र लिगेंड कहलाते है तथा ये निम्न चक्रण संकुल बनाते है।
- युग्मन ऊर्जा (P) > क्रिस्टल क्षेत्र विपाटन (Δo) हो तो इलेक्ट्रॉन eg कक्षक में जायेगा तथा जिन लिगेंड के कारण ऐसा होता है वे दुर्बल क्षेत्र लिगेंड कहलाते है तथा ये उच्च चक्रण संकुल बनाते है।
| क्र.स. | d – कक्षक में इलेक्ट्रॉन | लिगेंड | इलेक्ट्रॉनिक विन्यास | cfse का मान |
| 1 | d1 | प्रबल लिगेंड | t2g1 eg0 | 4dq |
| दुर्बल लिगेंड | t2g1 eg0 | 4dq | ||
| 2 | d2 | प्रबल लिगेंड | t2g2 eg0 | 8dq |
| दुर्बल लिगेंड | t2g2 eg0 | 8dq | ||
| 3 | d3 | प्रबल लिगेंड | t2g3 eg0 | 12dq |
| दुर्बल लिगेंड | t2g3 eg0 | 12dq | ||
| 4 | d4 | प्रबल लिगेंड | t2g4 eg0 | 16dq + 1P |
| दुर्बल लिगेंड | t2g3 eg1 | 6dq | ||
| 5 | d5 | प्रबल लिगेंड | t2g5 eg0 | 20dq + 2P |
| दुर्बल लिगेंड | t2g3 eg2 | 0dq | ||
| 6 | d6 | प्रबल लिगेंड | t2g6 eg0 | 24dq + 3P |
| दुर्बल लिगेंड | t2g4 eg2 | 4dq + 1P | ||
| 7 | d7 | प्रबल लिगेंड | t2g6 eg1 | 18dq + 3P |
| दुर्बल लिगेंड | t2g5 eg2 | 8dq + 2P | ||
| 8 | d8 | प्रबल लिगेंड | t2g6 eg2 | 12dq + 3P |
| दुर्बल लिगेंड | t2g6 eg2 | 12dq + 3P | ||
| 9 | d9 | प्रबल लिगेंड | t2g6 eg3 | 6dq + 4P |
| दुर्बल लिगेंड | t2g6 eg3 | 6dq + 4P | ||
| 10 | d10 | प्रबल लिगेंड | t2g6 eg4 | 0dq + 5P |
| दुर्बल लिगेंड | t2g6 eg4 | 0dq + 5P |
सामान्यतः लिगेंडो कों उनकी बढती हुई क्षेत्र प्रबलता के क्रम में निम्नानुसार एक श्रेणी (स्पेक्ट्रमी रासायनिक श्रेणी) में विभक्त किया गया है।
CO > CN– > en > NH3 > edta4- > NCS– > H2O > C2O22- > OH– > F– > S2- > Cl– > SCN– > Br– > I–
चतुष्फलकीय ज्यामिति के संकुलो मे d-कक्षकों का विपाटन
चतुष्फलकीय ज्यामिति के संकुलो मे d-कक्षकों का विपाटन अष्टफलकीय से उल्टा तथा कम होता है तथा ऊर्जा का मान Δt = 4/9Δo होता है अर्थात विपाटन ऊर्जा इतनी अधिक नही होती है कि इलेक्ट्रॉनों के युग्मन के लिए बाध्य करे अतः इस ज्यामिति के संकुल यौगिकों में निम्न चक्रण विन्यास न होकर उच्च चक्रण विन्यास ही मिलते है।
नोट
- 1.लिगेंड की अनुपस्थिति में क्रिस्टल क्षेत्र विपाटन नही होता है तथा पदार्थ रंगहीन होता है।
- [Ti(H2O)6]Cl3 को गर्म करने पर इसमें से जल का अणु वाष्पित हो जाता है जिससे यह रंगहीन हो जाता है।
- CuSO4 सफ़ेद होता है जबकि CuSO4.5H2O नीले रंग का होता है।
- 4.[Ni(H2O)6]2+ संकुल यौगिक का रंग हरा होता है यदि इसमें द्विदंतुक लिगेंड(en) को आण्विक अनुपातों 1:1, 2:1, 3:1 में मिला दिया जाये तो निम्न प्रकार इनका रंग परिवर्तित हो जाता है।
[Ni(H2O)6]2+ (हरा) + en → [Ni(H2O)4(en)]2+(हल्का नीला) + 2H2O
[Ni(H2O)4(en)]2+ (हल्का नीला) + en → [Ni(H2O)2(en)2]2+ (नीला)+ 2H2O
[Ni(H2O)2(en)]2+ (नीला) + en → [Ni(en)3]2+(बैंगनी) + 2H2O
क्रिस्टल क्षेत्र सिद्धांत की सीमाएँ
- ऋण आयनिक लिगेंड द्वारा d – कक्षको का विपाटन सर्वाधिक होना चाहिए जबकि स्पेक्ट्रो रासायनिक श्रेणी में ये निचले सिरे पर आते है।
- यह सिद्धांत लिगेंड और केन्द्रीय परमाणु के मध्य बंध की सहसंयोजक प्रवृति के बारे में नहीं बताता है।
wikipedia/Crystal_field_theory








1 Comment